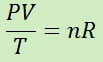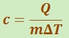1. Calor |
|
2. Temperatura |
|
3. Estados de la Materia |
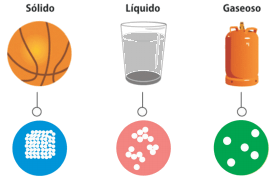
• Sólidos
• Líquidos • Gases • Gases Ideales Leyes Número de Avogadro mol mol-gramo Ecuación General • Cambios de Estado Puntos de Fusión, ebullición, congelación, condensación Calor Específico Calor Latente |
4. Mecanismos de Transferencia de Calor |
• Conducción
• Convección • Radiación |
5. Dilatación Térmica |
• Dilatación en Sólidos
• Dilatación en Líquidos Dilatación Anómala del Agua |
6. Leyes de la Termodinámica |
• Equilibrio Térmico (Ley Cero)
• Conservación de la Energía (Primera Ley) • Ley de la Entropia Creciente (Segunda Ley) • Ley del 0 absoluto inalcanzable (Tercera Ley) |
7. Curiosidades |
• ¿El color blanco es "fresco"?
• La manera más rápida de enfriar una bebida • ¿Cuál es la temperatura del fondo del mar? |
8. Recursos en la web |
• Videos
• Páginas web |
|
El Universo está hecho de materia y energía. La materia está compuesta de átomos y moléculas (agrupaciones de átomos) y la energía hace que los átomos y las moléculas estén siempre en movimiento, chocando entre sí o vibrando de un lado a otro.
|
|
Antes del siglo XIX el estudio del calor empleaba la caloría como su unidad de medida. Una caloría es la cantidad de energía necesaria para elevar la temperatura de un gramo de agua pura en 1°C a una presión de una atmósfera (nivel del mar).
A mediados del S. XIX el científico inglés James Prescott Joule diseñó un dispositivo con el cual estableció lo que se conoce como el equivalente mecánico del calor: |
A partir de entonces el calor se mide, al igual que otras formas de energía, en Joules.
Otras unidades de medición del calor • BTU es otra unidad de medida del calor; su nombre proviene de las iniciales de: British Thermal Unit (Unidad Térmica Británica) y se define como la cantidad de energía necesaria para elevar la temperatura de una libra (453.5924 gm) de agua pura en un grado Fahrenheit a una presión de una atmósfera. 1 BTU ↔ 1055 J
|
|
Los átomos y las moléculas en una sustancia no siempre viajan a la misma velocidad. Esto significa que hay un rango de energía (la energía del movimiento) entre las moléculas. En un gas, por ejemplo, las moléculas viajan en direcciones aleatorias a una variedad de velocidades, algunas son rápidas y otras lentas.
La energía térmica es la energía cinética promedio de un conjunto muy grande de átomos o moléculas. Esta energía cinética media depende de la temperatura, que se relaciona con el movimiento de las partículas (átomos y moléculas) que constituyen las sustancias. La energía térmica (calor) depende de la velocidad de las partículas, el número de partículas (el tamaño o la masa) y el tipo de partículas en un objeto. La temperatura no depende del tamaño o tipo de objeto. |
El calor hace que la temperatura aumenta o disminuya. Si agregamos calor, la temperatura aumentará; si lo eliminamos, ésta bajará. Temperaturas más altas significan moléculas moviendose, vibrando y rotando con más energía.
|
Escalas de Temperatura y Termómetros
|
Los termómetros son los dispositivos usados para medir la temperatura. La miden sobre una escala de temperatura que puede ser:
En la escala Fahrenheit (Gabriel Fahrenheit 1686-1736) el punto de congelación del agua se estableció en 32 grados y el punto de ebullición en 212 grados. Cada uno de los 180 grados (212-32) se denomina grado Fahrenheit [°F].
|
En la escala Centígrada o Celsius (Anders Celsius 1701-1744) los mismos puntos clave se establecieron en 0 grados y en 100 grados respectivamente. Cada uno de los 100 grados (100-0) se llama grado Centígrado [°C]. La escala Celsius se conoce como Unidad de Sistema Universal. Se usa en toda la ciencia y en la mayoría de los países.
La escala Kelvin o absoluta surge del descubrimiento realizado por Lord Kelvin de que hay un límite en lo frío que puede ser algo. Nada puede ser más frio que - 273 °C (exáctamente −273,15 °C). La escala Kelvin fija su cero en esta temperatura y cada grado, ahora llamado grado Kelvin o simplemente Kelvin [K], es un grado Centígrado por encima de dicha temperatura mínima posible. Para convertir entre las diferentes escalas se usan las siguientes relaciones: De K a °C °C = K-273 De °F a °C °C = (5/9) x (°F - 32) |
Existen distintas clases de termómetros según la magnitud física que se mide y que varía al variar la temperatura.
• Basados en la dilatación de:
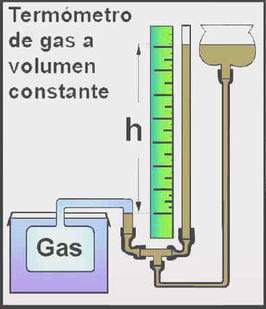
Gases: Aprovechando que, a presión constante, el volumen de un gas varía directamente con la temperatura o en que, a volumen constante, la presión de un gas varía directamente con la temperatura. Son muy exactos y generalmente son utilizados para la calibración de otros termómetros
Líquidos: Basados en la variación de la altura de una columna de un líquido que puede ser mercurio o alcohol coloreado.
Sólidos: El termómetro "bimetálico" consiste en dos placas de diferentes metales unidas rigidamente. El conjunto se dobla en arco de manera proporcional al cambio de temperatura. Esto se debe a que cada placa tiene un coeficiente de dilatación distinto y los cambios de temperatura provocan cambios distintos en sus longitudes
• Basados en propiedades eléctricas
En el "termómetro de platino" la resistencia eléctrica de un hilo de platino varía linealmente con la temperatura. El "termistor" es un semiconductor y, como tal, su conducción depende de la temperatura a la que se encuentre. En el Efecto termoeléctrico se fundamenta el "termopar" que es un par de empalmes (soldaduras) de dos alambres conductores de metales distintos. Uno de los empalmes se mantiene a una temperatura constante de referencia. La fuerza electromotriz generada depende de la diferencia de temperaturas entre las soldaduras.
• Basados en radiación térmica
Radiación infrarroja Termómetro infrarrojo: Los cuerpos calientes emiten calor en forma de radiaciones electromagnéticas, captada por este tipo de termómetros. Luz visible Pirómetro óptico: Son normalmente utilizados para medir temperaturas superiores a 700 ºC. Se basan en el cambio del color con el que brillan los objetos calientes. Desde el rojo oscuro al amarillo, llegando casi al blanco a unos 1300º C
• Basados en la dilatación de:
Gases: Aprovechando que, a presión constante, el volumen de un gas varía directamente con la temperatura o en que, a volumen constante, la presión de un gas varía directamente con la temperatura. Son muy exactos y generalmente son utilizados para la calibración de otros termómetros
Líquidos: Basados en la variación de la altura de una columna de un líquido que puede ser mercurio o alcohol coloreado.
Sólidos: El termómetro "bimetálico" consiste en dos placas de diferentes metales unidas rigidamente. El conjunto se dobla en arco de manera proporcional al cambio de temperatura. Esto se debe a que cada placa tiene un coeficiente de dilatación distinto y los cambios de temperatura provocan cambios distintos en sus longitudes
• Basados en propiedades eléctricas
En el "termómetro de platino" la resistencia eléctrica de un hilo de platino varía linealmente con la temperatura. El "termistor" es un semiconductor y, como tal, su conducción depende de la temperatura a la que se encuentre. En el Efecto termoeléctrico se fundamenta el "termopar" que es un par de empalmes (soldaduras) de dos alambres conductores de metales distintos. Uno de los empalmes se mantiene a una temperatura constante de referencia. La fuerza electromotriz generada depende de la diferencia de temperaturas entre las soldaduras.
• Basados en radiación térmica
Radiación infrarroja Termómetro infrarrojo: Los cuerpos calientes emiten calor en forma de radiaciones electromagnéticas, captada por este tipo de termómetros. Luz visible Pirómetro óptico: Son normalmente utilizados para medir temperaturas superiores a 700 ºC. Se basan en el cambio del color con el que brillan los objetos calientes. Desde el rojo oscuro al amarillo, llegando casi al blanco a unos 1300º C
|
El agua se puede encontrar como sólido (hielo), líquido (agua líquida) o gas (vapor de agua). Estos estados se denominan "fases". Una fase describe un estado físico de la materia.
En la Tierra, la mayor parte de las sustancias pueden clasificarse dentro de los tres primeros, puesto que el plasma no existe libremente en la superficie de la Tierra en condiciones normales. Se presenta en condiciones de altas temperaturas (más de 1500 ºC) y es un gas que posee una cantidad extra de partículas cargadas electricamente que se conoce como gas ionizado. En el universo, el 98% es plasma. Es el estado de la materia en las estrellas.
|
El plasma se puede generar artificialmente calentando un gas a una temperatura muy alta, lo que provoca colisiones tan vigorosas entre sus átomos y moléculas que los electrones quedan libres, produciendo la ionización.
|
|
Sólidos
Los átomos y moléculas en sólidos solo pueden rotar y vibrar (agitación térmica) alrededor de una posición de equilibrio; puede decirse que sus moléculas tienen mayor cantidad de energía potencial que de energía cinética (mayor fuerza de cohesión molecular que de repulsión). Debido a estas propiedades, los sólidos son rígidos, presentan forma propia y ofrecen cierta resistencia a las deformaciones.
Animación: http://itlrc.com/science
|
• No pueden comprimirse (mantienen su volumen). Algunos materiales son flexibles como el caucho y parecen comprimirse, pero solo aparéntemente ya que el material se expande en otro lugar ... otros materiales pueden tener espacios en ellos y solo parecen comprimirse a medida que las moléculas se introducen en estos espacios.
• Mantienen su volumen, forma y tienen superficies bien definidas • Muestran poca o ninguna evaporación. |
|
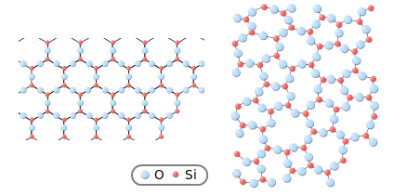
En la naturaleza casi todos los sólidos son cristalinos (se presentan en forma de cristales); sus propiedades dependerán de la diferencia en sus estructuras cristalinas. Por ejemplo, los átomos de carbono pueden constituirse de dos maneras diferentes, para formar grafito o bien para formar diamante.
Algunos sólidos que no presentan en su estructura interna la regularidad de los cristales, se conocen como amorfos, por ejemplo el vidrio, el asfalto o el caucho. |
Dependiendo del proceso de solidificación un mismo compuesto puede formar una red cristalina o un sólido amorfo. Por ejemplo, según la disposición espacial de las moléculas del sílice (dióxido de silicio SiO2), se puede obtener una estructura cristalina (el cuarzo) o un sólido amorfo (el vidrio).
|
Líquidos
Animación: http://itlrc.com/science
|
• No pueden comprimirse (mantienen su volumen).
• No mantienen su forma. Se adaptan a la forma del recipiente que los contiene. • Su superficie está definida (tensión superficial). • Pueden evaporarse. |
El movimiento de vibración de los átomos se hace con mayor libertad, permitiendo que existan pequeñas traslaciones. A ello se debe que los líquidos puedan escurrir o fluir. No ofrecen resistencia a la deformación —adoptan la forma del recipiente que los contiene— y son incompresibles.
En ciertos líquidos, existe una estructura localmente ordenada, lo que da origen a cristales líquidos, como los que se utilizan en las pantallas LCD de las calculadoras, computadoras y televisores.
En ciertos líquidos, existe una estructura localmente ordenada, lo que da origen a cristales líquidos, como los que se utilizan en las pantallas LCD de las calculadoras, computadoras y televisores.
|
Gases
Animación: http://itlrc.com/science
La fuerza de cohesión entre los átomos es prácticamente nula y predomina la energía cinética sobre la potencial.
|
• Tienden a ocupar el mayor volumen posible, por lo que su densidad es variable.
• Pueden comprimirse, como cuando por ejemplo en una jeringa cerrada se presiona con el émbolo el aire dentro de ella y éste disminuye en volumen; una vez que el émbolo se suelta, el aire vuelve a expandirse a su máxima capacidad. • Tienen una relación definida entre el volumen, la presión y la temperatura de un gas, de modo que una cantidad de gas ocupa un volumen bien determinado a una presión y temperatura dadas. Aunque esta relación es muy compleja para un gas denso, es muy simple para un gas ideal. Las propiedades de los gases ideales son importantes en la práctica porque los gases que intervienen en la respiración son aproximadamente ideales. |
|
Los gases pueden ser monoatómicos o diatómicos según estén compuestos de un solo átomo o de dos. Todos los gases nobles [Helio (He), Neón (Ne), Ar (Argón), Kr (Kriptón), Xe (Xenón) y Radón (Rn)] son monoatómicos. Los otros elementos elementos que normalmente, a temperatura ambiente, se encuentran en estado gaseoso, suelen estarlo en forma de moléculas diatómicas. Estas se nombran con el nombre del elemento.
|
Tabla: 94jechm.wordpress.com
|
Gases Ideales
|
|
Los gases tienen un comportamiento ideal cuando se encuentran a bajas presiones y temperaturas moderadas, en las cuales se mueven lo suficientemente alejadas unas de otras, de modo que se puede considerar que sus moléculas no interactúan entre si (no hay acción de las fuerzas intermoleculares).
|
Leyes de los Gases Ideales
|
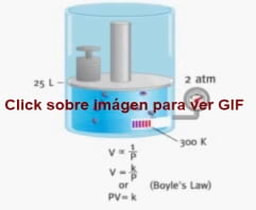
Ley de Boyle-Mariotte:
|
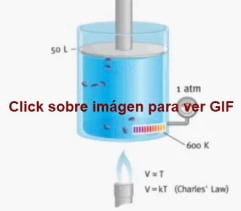
Ley de Charles:
|
|
Ley de Gay-Lussac:
|
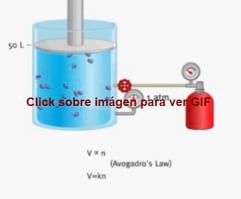
Ley de Avogadro:
|
Número de Avogadro
El número de Avogadro (NA) es el número de átomos o moléculas que existen en un mol de un elemento o compuesto
NA = 6.022 • 1023 partículas/mol
El número de Avogadro es enorme, equivale aproximadamente al volumen de la luna dividido en bolas de 1 milímetro de radio. Recibe ese nombre por el científico italiano Amedeo Avogadro, quien, dijo que el volumen de un gas es proporcional al número de átomos, o moléculas.
NA = 6.022 • 1023 partículas/mol
El número de Avogadro es enorme, equivale aproximadamente al volumen de la luna dividido en bolas de 1 milímetro de radio. Recibe ese nombre por el científico italiano Amedeo Avogadro, quien, dijo que el volumen de un gas es proporcional al número de átomos, o moléculas.
mol
Un mol es la cantidad de materia que contiene el número de Avogadro de partículas elementales (ya sean átomos, moléculas, iones, partículas subatómicas, etc.)
6.022 • 1023 átomos ↔ 1 mol de átomos
NA átomos ↔1 mol de átomos
6.022 • 1023 átomos ↔ 1 mol de átomos
NA átomos ↔1 mol de átomos
|
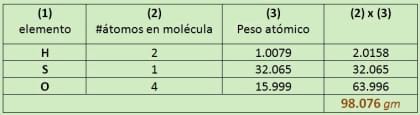
átomo-gramo
Es la masa de un mol de átomos (NA átomos) de un elemento. Esta masa es exactamente igual al peso atómico del elemento expresado en gm. |
La tabla periódica de elementos que se usó para estos ejemplos la encuentar aquí: tabla periódica
|
Ecuación General de los gases ideales
|
Paul Emile Clapeyron (1799-1844) estableció una relación entre las variables de estado con la siguiente expresión matemática:
PV = nRT P es la presión a la que está sometido el gas V es el volumen que ocupa T es la temperatura absoluta del gas n es el número de moles del gas R es la constante universal de los gases ideales que puede asumir diferentes valores según las unidades de medida empleadas como se muestra en la siguiente tabla: |
A partir de la ecuación de Clapeyron, podemos establecer la siguiente relación:
Como el número de moles n y R son constantes, se concluye que si variamos la presión, el volumen y la temperatura de una misma cantidad de gas la relación PV/T dará el mismo resultado.
|
Cambios de estado
|
Los cambios de fase reciben diferentes nombres según las fases entre las que ocurren y de si se está añadiendo a sustrayendo energía.
|
Sublimación: es el proceso que consiste en el cambio de estado de sólido al estado gaseoso sin pasar por el estado líquido. . Un ejemplo de tales sustancias es el dióxido de carbono (CO2) sólido o hielo seco el cual sublima a la temperatura ambiente. Cristalización (sublimación inversa): es el proceso inverso a la sublimación progresiva, es decir, el paso directo de gas a sólido.
|
Puntos de Fusión, Ebullición, Condensación, Congelación
|
|
El punto de ebullición, de una sustancias depende de la presión y de la pureza de la sustancia.
|
El punto de ebullición del agua es 100 ºC. pero esto solo si lo medimos a una presión de 1 atmósfera (la presión atmosférica al nivel del mar). La presión atmosférica es el peso del aire que tenemos sobre nosotros. Es fácil de deducir por lo tanto que cuanto menos aire haya sobre nuestra cabeza, menos presión hará el aire sobre ella.
El agua hierve (cambia del estado líquido al gaseoso) a menor temperatura cuanto menor sea la presión atmosférica, es decir cuanto menor sea la altura sobre el nivel del mar. En un lugar como Bogota (2630 m) el agua cuando hierbe lo hace a una menor temperatura. Esto se traduce en que la cocción de los alimentos tome más tiempo. En una olla a presión se eleva la presión sobre el agua para que así a las moléculas de agua que se escapan del líquido encuentran una mayor presión que vencer y requieran más energía (calor) para hacerlo.
|
La diferencia entre el punto de ebullición de la solución y el del disolvente puro para una presión constante establecida, se conoce como elevación del punto de ebullición. Esta elevación depende de la naturaleza del disolvente y de la concentración del soluto, pero es independiente, por lo menos en soluciones diluidas, de la naturaleza del soluto en tanto este no se disocie.
El punto de ebullición del agua pura es 100°C, pero ese punto de ebullición puede ser elevado por la adición de un soluto tal como una sal. Una solución tiene típicamente un punto de ebullición más alto que el medible en el disolvente puro.
| ||||||||||||||||||||||||||||||
Calor Específico (c) y Calor Latente
Cuanto mayor es el calor específico de una sustancia, más calor hay que suministrarle (o sustraerle) para conseguir variar su temperatura. Viene dada por:
|
Donde c (minúscula) es el calor específico, m es la masa y ΔT es la diferencia de temperatura; las unidades usuales son ( Kcal / Kg‧°C ) ó ( J / Kg‧°C ). Si despejamos Q obtenemos la ecuación fundamental de la termología:
Q = m‧ c‧ ΔT Con ella podemos determinar el calor que se debe agregar o sustraer a una sustancia para incrementar su temperatura si se conoce el calor específico y la cantidad de masa. Nota: siempre y cuando el incremento de temperatura esté dentro del rango en que la sustancia permanece en el mismo estado. |
Tabla encontrada en: http://mmramorporelsaber
|
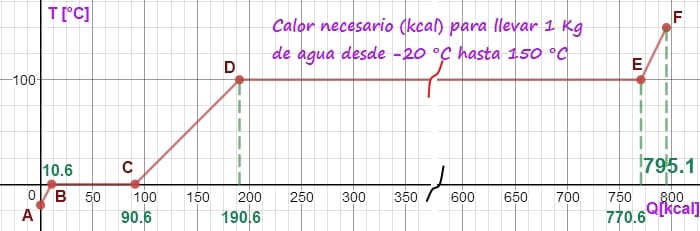
Imaginemos un experimento que consista en aplicar calor a un recipiente con un cubo de hielo a - 20 °C y de masa es 1 Kg hasta que la temperatura del vapor de agua sea 150 °C
AB
: El calor calor hace que la temperatura suba desde -20°C hasta 0°C; el calor necesario está dado por:
Q = m‧ ceh‧ ∆T
Donde m es la masa de hielo, ceh es el calor específico del hielo y ∆T es la diferencia de temperatura ( Tf - To ). Reemplazando valores:
Q = 1 ∙ 0.53 ∙ 20 = 10.6 kcal
BC : La temperatura permanece en 0 °C mientras todo el cubo de hielo se funde (derrite) por completo. El calor, suministrado durante este lapso, no se utiliza para aumentar la temperatura del cuerpo, sino para producir su fusión. Por eso se llama "calor latente de fusión"; dado por:
Q = m‧ clfa
Donde m es la masa de hielo a 0 °C y clfa es el calor latente de fusión del agua. Reemplazando valores:
Q = 1 ∙ 80 = 80 kcal
CD : Cuando todo el hielo se ha convertido completamente en agua líquida a 0°C, la temperatura de ésta comienza a elevarse nuevamente hasta alcanzar el siguiente punto de cambio de estado que, para el agua, son 100°C; la cantidad de calor necesaria para lograrlo está dada por:
Q = m‧ cea‧ ∆T
Donde m es la masa de agua líquida, cea es el calor específico del agua líquida y ∆T es la diferencia de temperatura ( Tf - To ). Reemplazando valores:
Q = 1 ∙ 1 ∙ 100 = 100 kcal
DE : La temperatura permanece en 100 °C mientras el agua líquida se evapora por completo. El calor, suministrado durante ese lapso, no se utiliza para aumentar la temperatura del cuerpo, sino para producir su vaporización. Por eso se llama "calor latente de vaporización". Está dado por
Q = m‧ clva
Donde m es la masa de hielo a 0 °C y clva es el calor latente de vaporización del agua. Reemplazando valores:
Q = 1 ∙ 580 = 580 kcal
EF : Una vez que todo el agua líquida se ha evaporado por completo, la temperatura, en este caso del vapor, comienza a elevarse nuevamente desde 100 °C hasta llegar a la temperatura deseada (150 °C). El calor necesario es:
Q = m‧ cev‧ ∆T
Donde m es la masa de vapor, cev es el calor específico del vapor de agua y ∆T es la diferencia de temperatura ( Tf - To ). Reemplazando valores:
Q = 1 ∙ 0.49 ∙ 50 = 24.5 kcal
Q = m‧ ceh‧ ∆T
Donde m es la masa de hielo, ceh es el calor específico del hielo y ∆T es la diferencia de temperatura ( Tf - To ). Reemplazando valores:
Q = 1 ∙ 0.53 ∙ 20 = 10.6 kcal
BC : La temperatura permanece en 0 °C mientras todo el cubo de hielo se funde (derrite) por completo. El calor, suministrado durante este lapso, no se utiliza para aumentar la temperatura del cuerpo, sino para producir su fusión. Por eso se llama "calor latente de fusión"; dado por:
Q = m‧ clfa
Donde m es la masa de hielo a 0 °C y clfa es el calor latente de fusión del agua. Reemplazando valores:
Q = 1 ∙ 80 = 80 kcal
CD : Cuando todo el hielo se ha convertido completamente en agua líquida a 0°C, la temperatura de ésta comienza a elevarse nuevamente hasta alcanzar el siguiente punto de cambio de estado que, para el agua, son 100°C; la cantidad de calor necesaria para lograrlo está dada por:
Q = m‧ cea‧ ∆T
Donde m es la masa de agua líquida, cea es el calor específico del agua líquida y ∆T es la diferencia de temperatura ( Tf - To ). Reemplazando valores:
Q = 1 ∙ 1 ∙ 100 = 100 kcal
DE : La temperatura permanece en 100 °C mientras el agua líquida se evapora por completo. El calor, suministrado durante ese lapso, no se utiliza para aumentar la temperatura del cuerpo, sino para producir su vaporización. Por eso se llama "calor latente de vaporización". Está dado por
Q = m‧ clva
Donde m es la masa de hielo a 0 °C y clva es el calor latente de vaporización del agua. Reemplazando valores:
Q = 1 ∙ 580 = 580 kcal
EF : Una vez que todo el agua líquida se ha evaporado por completo, la temperatura, en este caso del vapor, comienza a elevarse nuevamente desde 100 °C hasta llegar a la temperatura deseada (150 °C). El calor necesario es:
Q = m‧ cev‧ ∆T
Donde m es la masa de vapor, cev es el calor específico del vapor de agua y ∆T es la diferencia de temperatura ( Tf - To ). Reemplazando valores:
Q = 1 ∙ 0.49 ∙ 50 = 24.5 kcal
Sumando las kcal necesarias en cada paso, resulta que se requieren 795.1 kcal para llevar 1 Kg de hielo a -20 °C hasta vapor de agua a 150 °C
Tabla encontrada en: http://slideplayer.es/slide/1515880/
|
Hay videos en recursos_web
|
Con este conocimiento usted está en capacidad de resolver problemas como los siguientes:
Conducción
|
En la conducción dos cuerpos que se encuentran directamente en contacto (o partes de un mismo cuerpo a distinta temperatura) e intercambian energía sin que exista transporte de materia. Se basa en la transferencia directa de energía cinética a escala molecular.
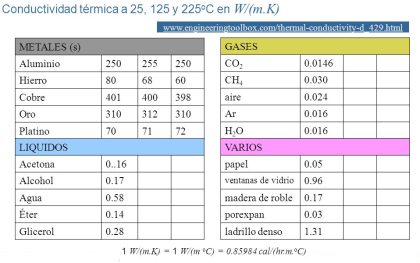
Cada sustancia posee una conductividad térmica que indica la rapidez con que es capaz de transferir la energía. Su unidad de medida en el Sistema Internacional es el watio por metro y por grado kelvin ( W/m·°K ). Los materiales pueden ser:
• Buenos conductores térmicos si poseen una alta conductividad. • Malos conductores térmicos si poseen una baja conductividad. Tabla encontrada en: http://slideplayer.es/slide/164861/
Otras tablas en: https://es.slideshare.net |
Hay videos en recursos_web
|
Convección
|
Se produce en líquidos y gases. En este caso si existe transporte de materia. El calor se propaga debido a unas corrientes denominadas corrientes de convección que se producen entre las distintas partes de la sustancia. Aquellas a mayor temperatura (por estar en contacto con la fuente de calor) disminuyen su densidad respecto a las más frías. Las partes menos densas (más calientes) se desplazan a las capas altas y las más densas (más frías) a las bajas.
Al cabo del tiempo, se repite el proceso al enfriarse las capas superiores y calentarse las inferiores, dando lugar así a una corriente de convección. Este fenómeno se da, por ejemplo, cuando calentamos un agua en una olla.
|
Hay videos en recursos_web
|
Radiación
Radiación viene de rayo, que significa "recta naciente", y es la emanación y propagación rectilínea, sin que sea necesaria la presencia de materia, de un flujo de partículas u ondas, que pueden ser materiales (tener masa en reposo, como la radiación de electrones, de protones, de neutrones, de partículas a (núcleos de helio), de partículas P (electrones provenientes del núcleo), de iones, etc.) o partículas energéticas sin masa, llamadas fotones, y que corresponden a las ondas electromagnéticas.
El espectro electromagnético (o simplemente espectro) es el rango de todas las radiaciones electromagnéricas posibles. El espectro de un objeto es la distribución característica de la radiación electromagnética de ese objeto. Se extiende desde las bajas frecuencias usadas para la radio moderna (extremo de la onda larga) hasta los rayos gamma (extremo de la onda corta), que cubren longitudes de onda de entre miles de kilómetros y la fracción del tamaño de un átomo.
Las radiaciones que dan lugar a efectos térmicos en su interacción con la materia están en la banda de 10-7< λ <10-4 m (ultravioleta, visible e infrarrojo).
El espectro electromagnético (o simplemente espectro) es el rango de todas las radiaciones electromagnéricas posibles. El espectro de un objeto es la distribución característica de la radiación electromagnética de ese objeto. Se extiende desde las bajas frecuencias usadas para la radio moderna (extremo de la onda larga) hasta los rayos gamma (extremo de la onda corta), que cubren longitudes de onda de entre miles de kilómetros y la fracción del tamaño de un átomo.
Las radiaciones que dan lugar a efectos térmicos en su interacción con la materia están en la banda de 10-7< λ <10-4 m (ultravioleta, visible e infrarrojo).
|
Cuando el Sol calienta la Tierra, su energía recorre una gran distancia en el espacio vacío. El sol es un claro ejemplo de cuerpo que emite radiación electromagnética debido a su temperatura. Sin embargo todos los cuerpos, por el hecho de encontrarse a cierta temperatura, emiten radiación térmica. Dicha radiación es de naturaleza electromagnética y, en el caso de los cuerpos muy calientes, como el sol, está dentro del rango de luz visible. Para otros objetos la radiación es invisible a nuestros ojos.
|
Hay videos en recursos_web
|
Radiación del Cuerpo Humano
Es el proceso por el cual los cuerpos aumentan su volumen debido a su temperatura. Cuando un cuerpo aumenta su temperatura, las partículas se mueven más deprisa, por lo que necesitan más espacio para desplazarse. Es por ello que el cuerpo necesita aumentar su volumen.
Dilatación en Sólidos
De entre los estados de agregación de la materia estudiados, el estado sólido es el que tiene las fuerzas de cohesión más fuertes, por lo que resulta más dificil observar la dilatación que en líquidos y gases. En función del número de dimensiones que predominan en el cuerpo, podemos distinguir tres casos:
De entre los estados de agregación de la materia estudiados, el estado sólido es el que tiene las fuerzas de cohesión más fuertes, por lo que resulta más dificil observar la dilatación que en líquidos y gases. En función del número de dimensiones que predominan en el cuerpo, podemos distinguir tres casos:
|
Dilatación Lineal
Se produce cuando predomina una dimensión frente a las otras dos. Ejemplos de cuerpos que se dilatan linealmente son: varillas, alambres, barras... La dilatación lineal de un cuerpo viene dada por la expresión: lf = l0‧(1+α‧ΔT)
lf, l0 : Longitud final e inicial del cuerpo. ( m )
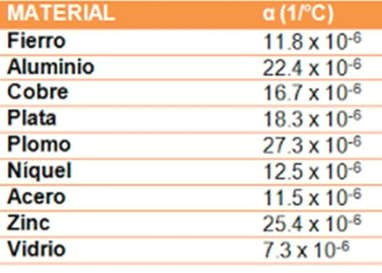
α : Coeficiente de dilatación lineal. Es específico de cada material y representa el alargamiento que experimenta la unidad de longitud de un sólido, cuando su temperatura se eleva 1 K. Su unidad de medida en el Sistema Internacional es el 1/°K, aunque también se usa el 1/°C ∆T : Incremento de temperatura que experimenta el cuerpo. Su unidad de medida en el Sistema Internacional es el grado kelvin ( °K ), aunque también se usa el ºC |
Hay videos en recursos_web
|
Dilatación Superficial
Se produce cuando predominan dos dimensiones (una superficie) frente a una tercera. Ejemplos de cuerpos que se dilatan superficialmente son: láminas, planchas... La dilatación superficial de un cuerpo viene dada por la expresión:
Se produce cuando predominan dos dimensiones (una superficie) frente a una tercera. Ejemplos de cuerpos que se dilatan superficialmente son: láminas, planchas... La dilatación superficial de un cuerpo viene dada por la expresión:
|
Af = A0‧(1+2α‧ΔT)
Af, A0 : Área final e inicial del cuerpo. ( m² )
α : Coeficiente de dilatación lineal. ∆T : Incremento de temperatura que experimenta el cuerpo. Si una lámina tiene un orificio, su diámetro aumentará cuando se la caliente.
|
Hay videos en recursos_web
|
Dilatación Volumétrica o Cúbica
Se produce cuando las tres dimensiones del cuerpo son igualmente relevantes. Ejemplos de cuerpos que se dilatan de modo volumétrico son: los dados del parchís, o las estatuas de los jardines ...
Se produce cuando las tres dimensiones del cuerpo son igualmente relevantes. Ejemplos de cuerpos que se dilatan de modo volumétrico son: los dados del parchís, o las estatuas de los jardines ...
|
Vf = V0‧(1+3α‧ΔT)
Vf, V0 : Volúmen final e inicial del cuerpo. ( m² )
α : Coeficiente de dilatación lineal. ∆T : Incremento de temperatura que experimenta el cuerpo. Un vaso, al calentarse, aumentará su volúmen.
|
Hay videos en recursos_web
|
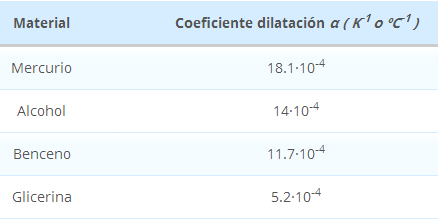
Dilatación en Líquidos
|
El efecto de la dilatación en los líquidos es más evidente que en los sólidos: al encontrarse sus moléculas con más libertad para moverse, el volumen que ocupa cada una aumenta más facilmente con la temperatura, por lo que también lo hace el volumen del líquido en su conjunto. Su expresión es:
V=V0‧(1+α‧ΔT)
|
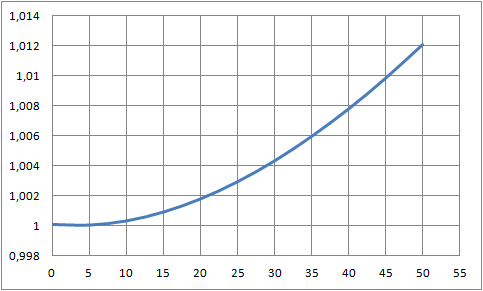
Dilatación anómala del agua
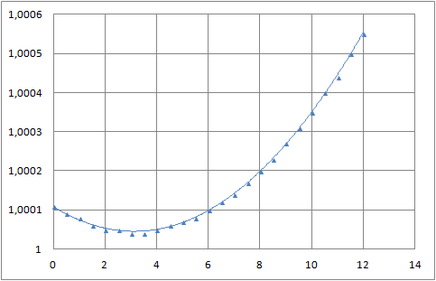
Los líquidos se caracterizan por dilatarse al aumentar la temperatura. Si observamos la gráfica anterior parecería que también es el caso del agua. Sin embargo el agua, no se comporta como los otros líquidos. Hagamos un "zoom" a la gráfica anterior en las proximidades de 0 °C.
|
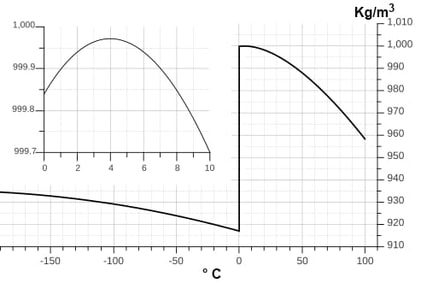
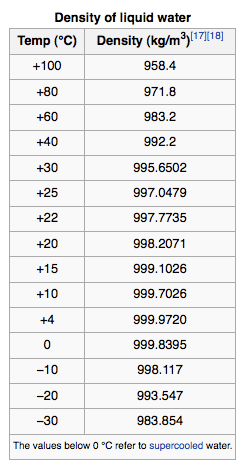
Este es el llamado comportamiento anómalo del agua y es de suma importancia para la preservación de la vida. La densidad del agua tiene un máximo a 4ºC, donde su valor* es de 1.000 gm/cm³. A cualquier otra temperatura su densidad es menor. Este comportamiento del agua es la razón por la que en los lagos se congela primero la superficie, y es en definitiva lo que hace posible la vida subacuática. Se recomienda ver, en la sección curiosidades, el video "¿Cuál es la temperatura del fondo del mar?"
By Klaus-Dieter Keller, created with QtiPlot, Font: Liberation Sans [CC BY-SA 3.0], from Wikimedia Commons
|
Foto: http://butane.chem
|
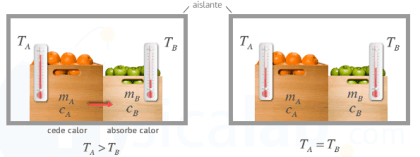
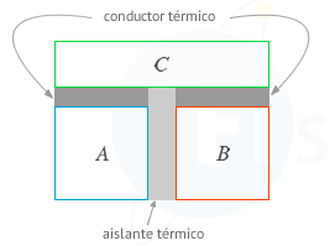
Equilibrio Térmico (Ley Cero)
|
Hay videos en recursos_web
|
Conservación de la Energía (Primera Ley)
Q=ΔU+W
• Q energía, en forma de calor, que el sistema recibe o dá (+ si recibe, - si dá); se expresa en calorias (cal) o Joules (J)
• ΔU cambio de la energía interna del sistema; se expresa en Joules (J)
• W energía, en forma de trabajo, que el sistema suministra o recibe (+ si entrega, - si recibe); se expresa en Joules (J)
• ΔU cambio de la energía interna del sistema; se expresa en Joules (J)
• W energía, en forma de trabajo, que el sistema suministra o recibe (+ si entrega, - si recibe); se expresa en Joules (J)

La primera ley expresa que el calor, suministrado por el medio ambiente (el quemador de la cocina) a un sistema (el agua contenida en el recipiente) es igual al cambio de la energía interna en el interior del liquido (agua en este caso) sumada al trabajo que el agua realiza cuando al hervir mueve la tapa contra el medio ambiente.
|
Hay videos en recursos_web
|
Ley de la entropía creciente (Segunda Ley)
La entropía en Termodinámica
En termodinámica, se define la entropía como la «energía no aprovechable» para realizar un trabajo. Es decir, una energía que está ahí, pero que no podemos utilizar. No podemos transformar el 100% del calor en energía aprovechable.
El primer principio de la termodinámica dice que la energía ni se crea ni se destruye entonces...
Si yo pongo en contacto un líquido caliente con uno frío (sistema inicial), el calor espontaneamente pasa del líquido caliente al líquido frio, calentándose este y enfriándose aquel (sistema final). Si deseara volver al sistema inicial no lo podría hacer espontaneamente, necesitaría una fuente de energía externa, pero además la energía necesaria para volver el liquido caliente a su estado inicial es mayor que la que energía que cedió al frío ya que una parte del calor que fluyo hacia el líquido frio se disipó en el ambiente calentándolo. Esta energía "se perdió" y constituye la entropía.
La 2ª ley establece que es imposible convertir completamente toda la energía de un tipo en otro sin que haya pérdidas. En todo proceso, perderemos algo de energía que no podremos aprooechar, en forma de calor que elevará la temperatura de la máquina o del medio ambiente.
El total de energía asociada con una fuente térmica núnca puede transformarse completamente en trabajo útil. De aquí que todo el trabajo se puede convertir en calor pero no todo el calor puede convertirse en trabajo.
El primer principio de la termodinámica dice que la energía ni se crea ni se destruye entonces...
Si yo pongo en contacto un líquido caliente con uno frío (sistema inicial), el calor espontaneamente pasa del líquido caliente al líquido frio, calentándose este y enfriándose aquel (sistema final). Si deseara volver al sistema inicial no lo podría hacer espontaneamente, necesitaría una fuente de energía externa, pero además la energía necesaria para volver el liquido caliente a su estado inicial es mayor que la que energía que cedió al frío ya que una parte del calor que fluyo hacia el líquido frio se disipó en el ambiente calentándolo. Esta energía "se perdió" y constituye la entropía.
La 2ª ley establece que es imposible convertir completamente toda la energía de un tipo en otro sin que haya pérdidas. En todo proceso, perderemos algo de energía que no podremos aprooechar, en forma de calor que elevará la temperatura de la máquina o del medio ambiente.
El total de energía asociada con una fuente térmica núnca puede transformarse completamente en trabajo útil. De aquí que todo el trabajo se puede convertir en calor pero no todo el calor puede convertirse en trabajo.
La entropía como una medida del "desorden"
Es muy fácil que las cosas se desordenen sin que hagamos mayor esfuerzo; se dice que la entropía aumenta. Para recuperar el órden (bajar la entropía) tenemos que invertir energía, tiempo, esfuerzo y dinero. Cuanto más he variado el sistema inicial (sistema ordenado), más trabajo me costará volver al estado inicial, he agregado más entropía al sistema (sistema más desordenado) y, no solo es más difícil volver al estado inicial cuanto más lo he cambiado, sino que quizás núnca lo logremos. Hemos hecho que el sistema sea irreversible.
Ejemplos de Sistema Irreversibles: Al romper un plato, hemos aumentado su entropía a un grado tal que ya no podremos dejarlo como estaba al principio. Del plato nuevo al roto se experimenta un gran aumento de la entropia. Freír un huevo es otro proceso irreversible.
Veamos un ejemplo más físico y real de un sistema irreversible. Si echamos una gota de tinta en agua observamos cómo ésta se difunde hasta que toda el agua se vuelve de color uniforme. Lo que jamás veremos es que las partículas de tinta se reúnan de nuevo en una gota separada del agua. Al cambiar el sistema inicial echando la gota de tinta, hemos aumentado tanto la entropia del sistema, que se vuelve irreversible.
Los procesos reales se producen en una dirección preferente. Es así como el calor fluye en forma espontánea de un cuerpo más cálido a otro más frío, pero el proceso inverso sólo se puede lograr con alguna influencia externa. Cuando un bloque desliza sobre una superficie, finalmente se detendrá. La energía mecánica del bloque se transforma en energía interna del bloque y de la superficie.
Ejemplos de Sistema Irreversibles: Al romper un plato, hemos aumentado su entropía a un grado tal que ya no podremos dejarlo como estaba al principio. Del plato nuevo al roto se experimenta un gran aumento de la entropia. Freír un huevo es otro proceso irreversible.
Veamos un ejemplo más físico y real de un sistema irreversible. Si echamos una gota de tinta en agua observamos cómo ésta se difunde hasta que toda el agua se vuelve de color uniforme. Lo que jamás veremos es que las partículas de tinta se reúnan de nuevo en una gota separada del agua. Al cambiar el sistema inicial echando la gota de tinta, hemos aumentado tanto la entropia del sistema, que se vuelve irreversible.
Los procesos reales se producen en una dirección preferente. Es así como el calor fluye en forma espontánea de un cuerpo más cálido a otro más frío, pero el proceso inverso sólo se puede lograr con alguna influencia externa. Cuando un bloque desliza sobre una superficie, finalmente se detendrá. La energía mecánica del bloque se transforma en energía interna del bloque y de la superficie.
La entropia no se puede medir en forma directa, es más fácil medir sus cambios.
Los sistemas naturales tienden, se comportan, dirigen sus cambios espontaneamente hacia una situación de equilibrio y se puede mostrar que dicha situación corresponde al máximo de entropía.
Los sistemas naturales tienden, se comportan, dirigen sus cambios espontaneamente hacia una situación de equilibrio y se puede mostrar que dicha situación corresponde al máximo de entropía.
El físico Rudolf Clausius (Koszalin, Prusia, 2 de enero de 1822- Bonn, 24 de agosto de 1888) en 1865, acuñó el término "entropia" (del griego ἐντροπή [entropḗ] «cambio», «giro») y llegó a una una fórmula para la entropía.
Según Clausius, el cambio de entropía ΔS de un sistema termodinámico que absorbe una cantidad de calor ΔQ a una temperatura absoluta T es simplemente la relación entre los dos:
Según Clausius, el cambio de entropía ΔS de un sistema termodinámico que absorbe una cantidad de calor ΔQ a una temperatura absoluta T es simplemente la relación entre los dos:
ΔS = ΔQ / T
Si un sistema experimenta un gran aumento de la entropía en el proceso de cambio, el sistema se vuelve irreversible.
La entropía es una cantidad que no decrece en ningún proceso físico, dando lugar a procesos que reciben el nombre de irreversibles, porque no se pueden deshacer, no es posible volver al estado de entropía anterior, dado que ésta no puede decrecer.
El calor no fluirá espontáneamente desde un objeto frío hacia un objeto caliente; se requiere ejercer un trabajo sobre el sistema para que esto se logre.
El segundo principio de la termodinámica establece que, si bien todo el trabajo mecánico puede transformarse en calor, no todo el calor puede transformarse en trabajo mecánico.
La entropía no está definida como una cantidad absoluta S (símbolo de la entropía), sino lo que se puede medir es la diferencia entre la entropía inicial de un sistema Si (antes de cambiarlo) y la entropía final del mismo Sf (después del cambio).
El segundo principio de la termodinámica establece que, si bien todo el trabajo mecánico puede transformarse en calor, no todo el calor puede transformarse en trabajo mecánico.
La entropía no está definida como una cantidad absoluta S (símbolo de la entropía), sino lo que se puede medir es la diferencia entre la entropía inicial de un sistema Si (antes de cambiarlo) y la entropía final del mismo Sf (después del cambio).
Ejemplos:
|
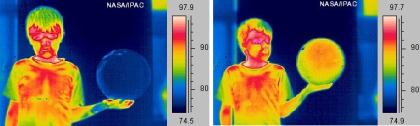
(1) La energía mecánica se convierte en energía térmica cada vez que rebota una pelota.
Cada vez que la pelota golpea el suelo, parte de la energía del movimiento de la pelota se convierte en calentamiento de la pelota, lo que hace que disminuya la velocidad en cada rebote. |
Una imagen infrarroja térmica de una bola antes (izquierda) y después (derecha) al rebotar.
|
|
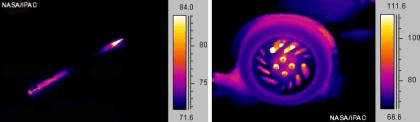
(3) La energía de la fricción crea calor.
Por ejemplo, cuando se frota las manos, afila un lápiz, hace una marca de patinazo con su bicicleta o usa los frenos de su auto, la fricción genera calor. |
Una imagen infrarroja térmica de un lápiz después de ser afilada (izquierda) y de frenos calientes en un automóvil (derecha). Observe la punta caliente del lápiz.
|
Ley del 0 Absoluto Inalcanzable (Tercera Ley)
Es el calor que entra desde el "mundo exterior" lo que impide que en los experimentos se alcancen temperaturas más bajas. El cero absoluto es la temperatura teórica más baja posible y se caracteriza por la total ausencia de calor. Es la temperatura a la cual cesa el movimiento de las partículas. El cero absoluto (0 K) corresponde aproximadamente a la temperatura de - 273,16ºC. Nunca se ha alcanzado tal temperatura y la termodinámica asegura que es inalcanzable.
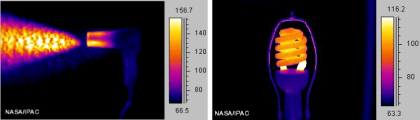
¿Qué tan "fresco" es el color blanco en verano?
|
Todos hemos escuchado que es mejor vestir de blanco para pasar menos calor en verano pero, ¿cómo de mejor es? En este vídeo se efectúa un experimento para que nos hagamos una idea.
|
Canal ciencia de sofá
|
¿Cuál es la manera más rápida de enfriar una bebida? (y por qué)
|
En este vídeo se ponen a prueba tres métodos que la gente suele utilizar para enfriar rápidamente sus bebidas: sumergiéndolas en a) hielo, b) en agua con hielo o c) en agua con hielo y sal. ¿Será verdad que el hielo con agua salada enfría las cosas más deprisa?
|
Canal ciencia de sofá
|
¿Cuál es la temperatura del fondo del mar?
|
Una buena explicación del comportamiento anómalo del agua y cómo está relacionado con la respuesta a esta pregunta.
|
Canal Rubiños
|
Videos
Páginas web
www.fisicalab.com
http://sems.gob.mx/work/models/sems/Resource/12179/8/images/cambios-fusion-ebullicion-agua.pdf
http://itlrc.com/science/scie4001/Unit%201-1%20States_of_Matter.html
http://ocw.uc3m.es/ciencia-e-oin/quimica-de-los-materiales/Material-de-clase/tema-4.-solidos-liquidos-y-disoluciones-ii/skinless_view
http://www.fullquimica.com/2012/02/mol-gramo-o-molecula-gramo-mol-g.html
https://nadiazg.wordpress.com/2012/04/06/volumen-de-una-mol-de-gas-ideal/
http://coolcosmos.ipac.caltech.edu//cosmic_classroom/light_lessons/thermal/index.html
https://www.engineeringtoolbox.com/water-density-specific-weight-d_595.html
http://corinto.pucp.edu.pe/quimicageneral/contenido/521-leyes-de-los-gases-ideales.html
www.vix.com/es/btg/curiosidades/4383/la-primera-ley-de-la-termodinamica
https://definicion.de/
http://coolcosmos.ipac.caltech.edu/cosmic_classroom/light_lessons/thermal/index.html
http://www.chem4kids.com/files/matter_states.html
http://www.areaciencias.com/fisica/entropia.html
http://jfinternational.com/mf/tercera-ley-termodinamica.html
http://slideplayer.es/slide/9413070/
http://sems.gob.mx/work/models/sems/Resource/12179/8/images/cambios-fusion-ebullicion-agua.pdf
http://itlrc.com/science/scie4001/Unit%201-1%20States_of_Matter.html
http://ocw.uc3m.es/ciencia-e-oin/quimica-de-los-materiales/Material-de-clase/tema-4.-solidos-liquidos-y-disoluciones-ii/skinless_view
http://www.fullquimica.com/2012/02/mol-gramo-o-molecula-gramo-mol-g.html
https://nadiazg.wordpress.com/2012/04/06/volumen-de-una-mol-de-gas-ideal/
http://coolcosmos.ipac.caltech.edu//cosmic_classroom/light_lessons/thermal/index.html
https://www.engineeringtoolbox.com/water-density-specific-weight-d_595.html
http://corinto.pucp.edu.pe/quimicageneral/contenido/521-leyes-de-los-gases-ideales.html
www.vix.com/es/btg/curiosidades/4383/la-primera-ley-de-la-termodinamica
https://definicion.de/
http://coolcosmos.ipac.caltech.edu/cosmic_classroom/light_lessons/thermal/index.html
http://www.chem4kids.com/files/matter_states.html
http://www.areaciencias.com/fisica/entropia.html
http://jfinternational.com/mf/tercera-ley-termodinamica.html
http://slideplayer.es/slide/9413070/